Ryder M, Pulcini E, Parker A, James G. Presented at the World Congress on Vascular Access, June 2016.
Streszczenie
Ryzyko zakażenia układu krwionośnego związane z urządzeniami dostępu naczyniowego i bezigłowymi zaworami budzi coraz większe zaniepokojenie. Pozostaje wiele pytań dotyczących potencjalnego ryzyka infekcji wśród różnych typów złączy. Dezynfekcja przed uzyskaniem dostępu ma ogromne znaczenie dla zapobiegania wnikania drobnoustrojów, ale przestrzeganie jej jest często niewystarczające. Badanie to oraz towarzysząca mu analiza statystyczna porównuje szybkość transferu bakterii przez 20 zaworów bezigłowych, oraz porównuje tworzenie się biofilmu wewnątrz zaworu, w łączniku cewnika i wewnątrz cewnika.
Model in vitro został zaprojektowany w celu symulacji czterokrotnego dziennie wlewu antybiotyków z wykorzystaniem metody podawania SASH (soli fizjologicznej, antybiotyku, soli fizjologicznej i heparyny). Podczas każdego, pięciodniowego badania łącznik każdego z zaworów był skażany dwa razy dziennie około 106 jednostkami tworzącymi kolonie (CFU) Staphylococcus aureus ATCC #6538. Po każdej inokulacji, zawory były przepłukiwane sześć razy, a z pierwszego i ostatniego przepłukiwania był robiony posiew i wyliczano bakterie. Zmierzono również średnie gęstości logarytmiczne (LD) CFU wewnątrz zaworu, w łączniku cewnika i wewnątrz cewnika.
Wyniki
Zawory Neutron® i MicroClave® wykazują najmniejszą średnią gęstość logarytmiczną bakterii w płynie po przepłukaniu w porównaniu z wszystkimi popłuczynami (= 3,14 i 3,20 loga(CFU/flush)). MicroClave i Neutron nie różniły się istotnie statystycznie i są jedynymi urządzeniami, które znajdowały się w grupie, która miała istotną statystycznie, najmniejszą średnią gęstość logarytmiczną bakterii w płynie po przepłukaniu.
Wnioski
Ryzyko przeniesienia bakterii przez zawór, w łącznik cewnika i światło cewnika do krwioobiegu z zanieczyszczonej powierzchni zaworu zależy od rodzaju zastosowanego zaworu. Analizy regresji sugerują, że log (CFU/złącze) jest najlepszym pojedynczym predyktorem średniej dobowej LD bakterii w popłuczynach (spośród trzech predyktorów: wewnątrz zaworu, w łączniku cewnika i wewnątrz cewnika.
Wprowadzenie
Poprzednie badania wskazują, że elementy konstrukcyjne zaworów bezigłowych wpływają na możliwość przedostania się bakterii z powierzchni zaworu do toru przepływu, łącznika cewnika i światła cewnika.1,2,3 Biofilm wewnątrz światła przewodu jest dominującym źródłem zakażeń krwiopochodnych (CRBSI) związanych z opieką nad cewnikiem
Cel
Celem pracy było porównanie szybkości transferu bakterii dla 20 zaworów bezigłowych oraz porównanie formowania się biofilmu wewnątrz zaworu, w łączniku cewnika i wewnątrz cewnika.
Metody
W pracy oceniono łącznie 20 konstrukcji zaworów bezigłowych. Cztery zawory każdego typu oceniono w trzech niezależnych badaniach (n=9), przy czym MicroClave służył, jako kontrola w każdej z 33 serii. Membrana zaworu była zakażana dwa razy dziennie około 106 CFU Staphylococcus aureus ATCC #6538. Zawór inokulowany był pozostawiony do wyschnięcia przez 30 minut, a następnie podłączano go do poliuretanowego cewnika centralnego umieszczanego na obwodzie (PICC) o długości 50 cm.
Każdy zestaw cewnik-zawór przepłukano 3,0 ml sterylnego roztworu soli fizjologicznej, który został zebrany i wysiany na płytkę (pierwsze płukanie). Zestawy cewnik-zawór przepłukano sterylnym roztworem soli fizjologicznej (NS) jeszcze dwa raz i zablokowano sterylnym bulionem Brain Heart Infusion Broth (BHI) na jedną godzinę. Następnie przepłukano z użyciem NS jeszcze trzy razy. Ostatnie płukanie zostało również wysiane na płytkę (ostatnie płukanie).
Zestawy cewnik-zawór były skażane po raz drugi każdego dnia po szóstym sterylnym przepłukiwaniu solą fizjologiczną, po czym następowała druga seria przepłukiwania, przeniesienia na płytkę i blokad dla łącznej liczby 18 aktywacji zaworu dziennie, co jest uznawane za rutynową liczbę aktywacji na Oddziale Intensywnej Terapii
Cała procedura była powtarzana codziennie w ciągu pięciu dni. Z wyłączeniem dni 4 i 5, gdy pobrano po 2 zestawy cewnik-zawór do badań mikrobiologicznych i mikroskopowych metodą niszczącą.
Analizę statystyczną przeprowadzono przy użyciu testów ANOVA i Tukey w celu określenia istotnych, średnich różnic gęstości logarytmicznej bakterii w popłuczynach, wewnątrz zaworu, w łączniku cewnika i wewnątrz cewnika, pomiędzy różnymi zaworami bezigłowymi. Zastosowano regresję liniową, wielokrotną w celu określenia, czy jakakolwiek kombinacja gęstości logarytmicznej bakterii wewnątrz zaworu, w łączniku cewnika i wewnątrz cewnika może w sposób istotny przewidzieć gęstość logarytmiczną bakterii w popłuczynach.
Wyniki
Zawory Neutron i MicroClave wykazują ogólnie najmniejszą średnią gęstość logarytmiczną bakterii w płynie po przepłukaniu wszystkich elementów systemu (=3,14 i 3,20 logarytmu (CFU/flush)). MicroClave i Neutron nie różniły się znacząco od siebie i są jedynymi urządzeniami, które znajdują się w grupie, która miała najmniejszą istotną, średnią gęstość logarytmiczną bakterii po przepłukaniu.
W zaworach Q‑Syte® i UltraSite® występowały znacznie większe średnie LD bakterii po przepłukaniu w porównaniu z innymi typami zaworów. (= 5,37 i 5,15 log (CFU/flush)). Q‑Syte i UltraSite nie różniły się istotnie (p = 0,9101).
TABELA 1: KWADRAT ŚREDNIEJ DZIENNEGO ZAGĘSZCZENIA BAKTERII W ROZTWORZE PO PRZEPŁUKANIU.
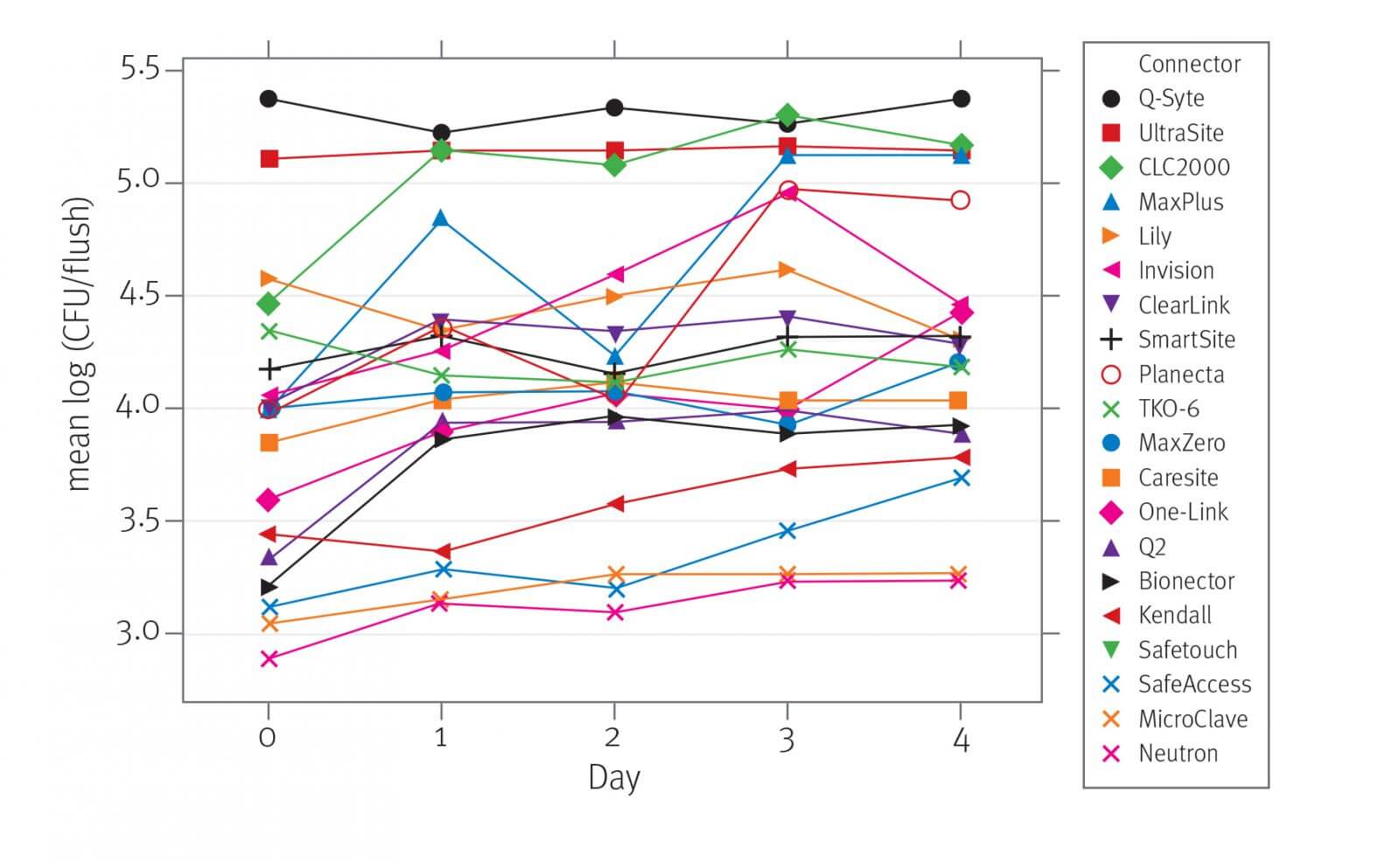
TABELA 2: ŚREDNIA KWADRATOWA PRZEPŁUKIWAŃ PRZEZ WSZYSTKIE DNI I WSZYSTKIE PRZEPŁUKIWANIA
.jpg)
Dyskusja
Ryzyko przeniesienia bakterii przez WNĘTRZE zaworu, łącznik cewnika i wewnątrz cewnika do krwioobiegu z zanieczyszczonej powierzchni zaworu zależy od jego typu. Wyniki badań potwierdzają, że powstawanie biofilmu w łączniku cewnika i w świetle cewnika może wynikać z transferu bakterii przez zawór bezigłowy. Wykazano ponadto, że oderwane lub planktoniczne bakterie oddzielające się od biofilmu są następnie wprowadzane do krwioobiegu za pomocą infuzji. Analiza regresji wskazuje, że tworzenie się biofilmu w zaworze było najlepszym predyktorem liczby bakterii wprowadzonych do krwioobiegu (R2 =95%). W ten sposób zastosowanie zaworu o niskiej szybkości transferu drobnoustrojów może zminimalizować ryzyko zakażenia krwiobiegu. Wskazuje również na stosowanie spójnych i skutecznych metod dezynfekcji zaworu i końcówki cewnika przed uzyskaniem dostępu, jako kluczowej strategii zapobiegania CRBSI. Dane sugerują również, że powszechna klasyfikacja dotycząca cech zaworów, takich jak podzielna membrana i zawór mechaniczny, jest zawodnym podejściem do wyboru urządzenia w oparciu o ryzyko infekcji.
Wnioski
Ryzyko przeniesienia bakterii ze skażonej powierzchni zaworu przez łącznik cewnika i światło cewnika do krwioobiegu zależy od rodzaju zastosowanego zaworu, a zawory MicroClave i Neutron wykazały znacznie niższe tempo przenoszenia bakterii niż jakiekolwiek inne badane zawory. Ponadto, częstotliwość wymiany zaworów może być zależna od potencjału przenoszenia bakterii w każdym projekcie urządzenia. Dane z tego badania wskazują również, że powszechna klasyfikacja podzielnej membrany i zaworu mechanicznego to zbyt uproszczone i zawodne podejście do doboru urządzenia w oparciu o ryzyko infekcji.
Bibliografia
- Brown JD, Moss HA, Elliott TSJ. The potential for catheter microbial contamination from a needleless connector. J Hosp Infect. 1997; 36:181–189
- Yebenes J, Delgado M, Sauca G, Serra-Prat M, Solsona M, Almirall J, et al. Efficacy of three different valve systems of needlefree closed connectors in avoiding access of microorganisms to endovascular catheters after incorrect handling. Crit Care Med 2008; 36: 2558–2561
- Ryder M, Fisher S, Hamilton G, Hamilton M, James G. Bacterial transfer through needlefree connectors: comparison of nine different devices. Presented at the Society for Healthcare Epidemiology of America Annual Scientific Meeting, April 2007
 English
English