Jak chronić siebie i innych przed rosnącą opornością na antybiotyki?

🏥 Zwracaj uwagę na pochodzenie produktów medycznych
Szukaj certyfikowanych rozwiązań, które ograniczają emisje.

🧪 Ogranicz nadużywanie antybiotyków
Nie przyjmuj ich bez wyraźnego zalecenia lekarza.

📣 Dziel się wiedzą
Edukacja społeczeństwa to jeden z filarów walki z globalnym kryzysem zdrowotnym.
Czy powietrze, którym oddychamy, może przyczyniać się do globalnego kryzysu antybiotykooporności?
Nowe badania opublikowane w The Lancet Planetary Health (2023) wskazują na alarmujący związek między zanieczyszczeniem powietrza a rozprzestrzenianiem się genów oporności na antybiotyki. Odkrycie to otwiera nową perspektywę na walkę z jednym z najpoważniejszych zagrożeń zdrowotnych XXI wieku.
PM2,5 i elementy oporności antybiotykowej – niewidzialne zagrożenie
Zanieczyszczenie powietrza pyłem zawieszonym PM2,5 (cząstki o średnicy mniejszej niż 2,5 mikrometra) od lat łączy się z chorobami układu oddechowego, sercowo-naczyniowego czy nowotworami. Jednak według najnowszych analiz, PM2,5 może również przenosić elementy genetyczne odpowiedzialne za antybiotykooporność – tzw. antibiotic resistance elements (AREs).
Te mikroskopijne cząstki mogą działać jak nośniki bakterii opornych na leki oraz genów, które po przedostaniu się do organizmu – przez wdychanie, spożycie lub kontakt ze skażoną wodą czy żywnością – mogą zwiększać ryzyko trudnych do leczenia infekcji.
Źródła skażenia – od szpitali po przemysł medyczny
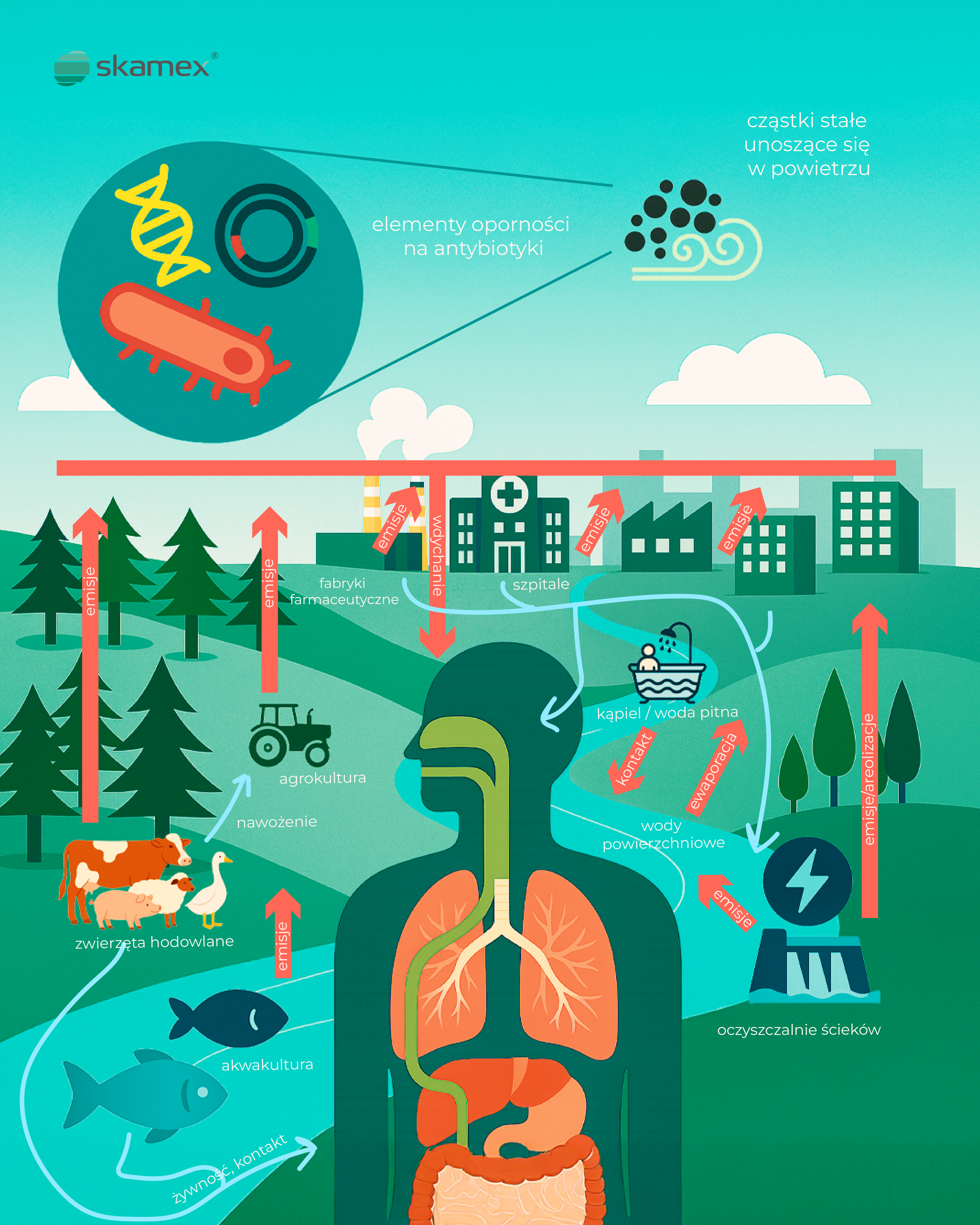
Schemat opublikowany w The Lancet Planetary Health przedstawia złożony system emisji i cyrkulacji AREs:
- Szpitale i fabryki farmaceutyczne emitują do atmosfery odpady zawierające leki i bakterie oporne.
- Społeczności miejskie i oczyszczalnie ścieków przyczyniają się do emisji, zarówno do powietrza, jak i do wód powierzchniowych.
- Rolnictwo i hodowla zwierząt – stosowanie antybiotyków prowadzi do przedostawania się ich pozostałości do gleby, wody, a przez pylenie – także do atmosfery.
- Akwakultura wprowadza antybiotyki do środowiska wodnego, które może trafiać do łańcucha pokarmowego.
- Producenci wyrobów medycznych, takich jak rękawice jednorazowe, którzy nie posiadają wdrożonych i certyfikowanych systemów zarządzania jakością, bezpieczeństwem i ochroną środowiska, mogą istotnie przyczyniać się do emisji PM2,5 – szczególnie jeśli korzystają z nieodnawialnych źródeł energii, np. z opalania węglem.
Ludzie mają kontakt z tymi zanieczyszczeniami na wiele sposobów – przez oddychanie, kontakt przez skórę, spożycie skażonej wody lub żywności, a nawet kąpiel w zanieczyszczonych zbiornikach.
Ukryte koszty ochrony zdrowia – nie każdy produkt chroni w pełni
Warto również podkreślić, że nawet działania podejmowane w celu ochrony zdrowia – jak stosowanie środków ochrony indywidualnej – mogą mieć negatywne konsekwencje, jeśli ich produkcja nie uwzględnia aspektów środowiskowych. Produkcja wyrobów medycznych bez niskoemisyjnych technologii, bez stosowania energii odnawialnej i bez nadzoru jakościowego może zwiększać zanieczyszczenie powietrza i pośrednio wspierać rozwój oporności bakterii.
Dlatego odpowiedzialne zakupy, oparte na certyfikacji i ekologicznych standardach produkcji, powinny być elementem polityki zrównoważonego rozwoju w ochronie zdrowia.
Innowacyjne rozwiązania w placówkach medycznych
W ramach ograniczania ryzyka transmisji bakterii opornych w środowisku medycznym, szczególnie w szpitalach i gabinetach, ważne jest stosowanie i wdrażanie odpowiednich środków ochrony indywidualnej. Najnowocześniejsze technologie produkcyjne pozwalają na wprowadzanie innowacyjnych rozwiązań, które gwarantują jego najwyższą jakość, bezpieczeństwo, jak również chronią środowisko.
Rozwiązaniem są rękawice, które łączą ochronę skóry z troską o środowisko.
Jednym z takich rozwiązań są rękawice posiadające warstwę ochronno-nawilżającą, która jest bezpieczna dla osób z atopowym zapaleniem skóry (AZS) oraz wymienione na liście produktów farmaceutycznych do ochrony skóry USP. Produkcja danych rękawic jest przy wdrożonych i certyfikowanych najwyższych standardach zarządzania jakości i bezpieczeństwa w myśli polityki zrównoważonego rozwoju w ochronie zdrowia, jak również przyczynia się do zmniejszenia ryzyka podrażnień i reakcji alergicznych u personelu medycznego.
Kolejnym rozwiązaniem są rękawice produkowane są z materiału nie zawierającego akceleratorów chemicznych ani siarki, co minimalizuje ryzyko wystąpienia alergii typu I i IV. Rękawice posiadają powłokę polimerową bez silikonu wykonaną z innowacyjnego materiału „SyNovus Plus”, który charakteryzują się wysoką odpornością zapewniającą doskonałą równowagę między wytrzymałością a miękkością, oferując użytkownikowi wysoki komfort noszenia. Cały proces produkcji odbywa się przy obniżonej emisji CO₂ w zakładach zasilanych energią odnawialną oraz opatrzone międzynarodowymi certyfikatami środowiskowymi, a sam materiał z którego wykonane są rękawice może być poddawany recyklingowi.
Zastosowanie obu rozwiązań w placówkach medycznych nie tylko chroni personel przed potencjalnymi alergenami i podrażnieniami, ale także zwiększa komfort pracy oraz ochrony przed potencjalnymi zagrożeniami związanymi z długotrwałym narażeniem na czynniki zewnętrzne.. W obliczu globalnych wyzwań związanych z antybiotykoopornością i zanieczyszczeniem powietrza, takie innowacyjne podejście do środków ochrony osobistej jest krokiem w kierunku zdrowszej przyszłości. Takie podejście pokazuje, że ochrona zdrowia może iść w parze z odpowiedzialnością za środowisko.
Wnioski i zalecenia
Badacze podkreślają, że wzrost stężenia PM2,5 może być odpowiedzialny za nawet 11% wzrost oporności bakterii w niektórych regionach świata. Co więcej, prognozy na kolejne dekady są alarmujące – do 2050 roku zanieczyszczenie powietrza może odpowiadać za setki tysięcy zgonów rocznie związanych z infekcjami odpornymi na leczenie.
Dlatego autorzy apelują o integrację polityki zdrowia publicznego z działaniami na rzecz ochrony środowiska. Kluczowe działania to:
• redukcja emisji pyłów zawieszonych PM2,5,
• poprawa zarządzania odpadami farmaceutycznymi,
• ograniczenie nadużywania antybiotyków w medycynie i rolnictwie,
• oraz promowanie niskoemisyjnej, certyfikowanej produkcji sprzętu medycznego, w tym środków ochrony indywidualnej.
Podsumowanie
Zanieczyszczenie powietrza to nie tylko problem klimatyczny czy pulmonologiczny – to także ukryty czynnik napędzający globalną antybiotykooporność. Nowe badania pokazują, jak złożone i wieloźródłowe są mechanizmy rozprzestrzeniania się genów oporności, i jak ważne jest systemowe podejście – obejmujące zdrowie ludzi, zwierząt i środowiska.
Czyste powietrze i czysta produkcja to nie tylko cele ekologiczne, ale i warunek skutecznej walki z globalnym kryzysem zdrowotnym.
Źródła:
1Zhu, Y.-G., Zhao, Y., Li, B., Huang, C.-L., Zhang, S.-Y., Yu, S., et al. (2023).
Air pollution and antibiotic resistance: A global relationship revealed by a multi-country study.
The Lancet Planetary Health, 7(9), e649–e659.
https://doi.org/10.1016/S2542-5196(23)00152–4
2World Health Organization (WHO). (2020).
Antimicrobial resistance and the environment: An emerging area of concern.
https://www.who.int/publications/i/item/9789240014472
3Chatterjee, A., Modarai, M., Naylor, N. R., Boyd, S. E., Atun, R., Barlow, J., & Holmes, A. H. (2018).
Quantifying drivers of antibiotic resistance in humans: a systematic review.
The Lancet Infectious Diseases, 18(12), e368–e378.
https://doi.org/10.1016/S1473-3099(18)30296–2
4Li, B., Yang, Y., Ma, L., Ju, F., Guo, F., Tiedje, J. M., & Zhang, T. (2015).
Metagenomic and network analysis reveal wide distribution and co-occurrence of environmental antibiotic resistance genes.
The ISME Journal, 9, 2490–2502.
https://doi.org/10.1038/ismej.2015.59
5Chen, Q.-L., An, X.-L., Li, H., Su, J.-Q., Ma, Y., & Zhu, Y.-G. (2016).
Long-term field application of sewage sludge increases the abundance of antibiotic resistance genes in soil.
Environment International, 92–93, 1–10.
https://doi.org/10.1016/j.envint.2016.03.026
6Ashbolt, N. J., Amezquita, A., Backhaus, T., Borriello, P., Brandt, K. K., Collignon, P., et al. (2013).
Human Health Risk Assessment (HHRA) for environmental development and transfer of antibiotic resistance.
Environmental Health Perspectives, 121(9), 993‑1001.
https://doi.org/10.1289/ehp.1206316
7van Bruggen, A. H. C., Finckh, M. R., & He, M. (2023).
Airborne routes of antibiotic resistance gene transmission in the environment.
Frontiers in Microbiology, 14, 1163212.
https://doi.org/10.3389/fmicb.2023.1163212
8European Centre for Disease Prevention and Control (ECDC). (2023).
Antimicrobial resistance surveillance in Europe 2023 – Annual report.
https://www.ecdc.europa.eu/en/antimicrobial-resistance/surveillance-and-disease-data/report
9OECD. (2022).
Tackling antimicrobial resistance: Ensuring sustainable investment in AMR.
Organisation for Economic Co-operation and Development.
https://www.oecd.org/health/tackling-antimicrobial-resistance.htm
9Kümmerer, K. (2009).
Antibiotics in the aquatic environment–a review–part I.
Chemosphere, 75(4), 417–434.
https://doi.org/10.1016/j.chemosphere.2008.11.086
10chrome-extension://efaidnbmnnnibpcajpcglclefindmkaj/https://www.sempermed.com/fileadmin/user_upload/MediaLibrary/Sempermed/Products/Examination_Gloves/Sempermed_green/FoldersBrochures_Sempermed_Green_Xfree_Datasheet_EN.pdf
11https://hartalega.com.my/sustainability/
12https://hartalega.com.my/speciality_type/colloidal-oatmeal-coated-gloves
 English
English



